Thể theo yêu cầu cuả admin BM, đồng thời để bảo đảm tính mạng (nếu ko BM quýnh mình chết ahhhh!!!!
.gif)
.gif)
), Bim sẽ post bài carben.
1.
Cấu trúc carben: Carben có hai dạng tồn tại: singlet và triplet. Dựa vào kết quả của phổ X-ray và EPR(electron paramagnetic resonance) ta thu được các thông số sau của 2 dạng carben:

Về cấu trúc điện tử của 2 dạng triplet và singlet, có 2 giả thuyết đưa ra:
-
giả thuyết 1: đối với dạng Singlet, carbon ở trạng thái lai hóa sp2, trong đó 2 e sẽ được điền vào orbital sp2 và còn 1 orbital p trống. góc liên kết R-C-R nhỏ hơn 120 độ do sự tương tác của cặp e trên orbital sp2, đối với dạng triplet, cacbon ở trạng thái lai hóa sp, hai e nằm ở hai orbital p.
-
giả thuyết 2: cà 2 dạng đều ở trạng thái lai hóa sp2. Đối với dạng singlet, 2 e ghép cặp đều nằm ở orbital sp2, nhưng đối với dạng triplet, 1 e ở obital sp2, e còn lại ở orbital p.
Bây giờ chúng ta sẽ cùng phân tích từng giả thuyết một !
-
giả thuyết 1: xét :CH2


-
giả thiết 2: cả 2 dạng của carbene đều ở trạng thái lai hóa sp2.


Với giả thuyết này ta có thể giải thích thỏa đáng các giá trị góc liên kết của triplet và singlet. Thật vậy, nếu carbon ở dạng triplet lai hóa sp, mỗi orbital p chứa 1 e độc thân chiếm vùng không gian rất nhỏ không thể dẩy góc liên kết H-C-H từ 180 độ về còn 130 – 150 độ. Nếu carbon này lai hóa sp2, góc liên kết bình thường H-C-H là 120 độ, nhưng do 1 orbital sp2 chứa 1 e độc thân chiếm vùng không gian nhỏ nên góc liên kết H-C-H có xu hướng mở rộng ra đến 130- 150 độ. Như vậy giả thiết 2 giải thích phù hợp với thực nghiệm hơn!
Ta xét gian đồ năng lượng phân tử của 2 dạng trên:


Về mức tương quan năng lượng giữa 2 dạng triplet và singlet được biểu thị qua giản đồ sau:

Sỡ dĩ ở trạng thái ground state, singlet có mức năng lượng cao hơn triplet là do tương tác đẩy của 2 e cùng nằm trong một orbital sp2.
Như vậy, một câu hỏi mới được đặt ra:
khi nào carbene tồn tại ở dạng triplet khi nào tồn tại ở dạng singlet? .gif)
Một lưu ý nhỏ cần quan tâm là cả 2 dạng của carbene đều có thế năng cao. Khi nói carbene này tồn tại chủ yếu ở dạng triplet điều đó có nghĩa là dạng triplet có năng lượng thấp hơn dạng singlet.
Nếu
carbon liên kết với những nhóm thế có cặp e tự do như O, Cl (chẳng hạn như :CCl2)
thì cacben tồn tại chủ yếu ở dạng nào? Khi có những nhóm thế có đặc tính như trên, cặp e p có khuynh hướng xen phủ với obital p của carbene. Nếu carbene ở dạng triplet, để sự xen phủ xảy ra thuận lợi, e p có khuynh hướng
ghép cặp với e trên orbital sp2. Năng lượng cần thiết để xảy ra sự ghép cặp e khoảng 40kJ/mol. Vì thế để thuận lợi về mặt năng lượng
carbene sẽ ở dạng singlet.

Ngoài ra, cấu trúc của cacben còn phụ thuộc vào cách thức tạo ra nó.Chẳng hạn như một trong những cách để điều chế carbene là pu khử
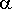
của hợp chất halogenur R2CH-X với sự hiện diện của 1 bazo mạnh hoặc hợp chất cơ kim.

Với pu này dạng carbene hình thành là singlet:

Nếu carbene hình thành là :CH2 và nếu pu xảy ra nhanh, dạng singlet vừa mới hình thành sẽ chuyển sang dạng triplet.Như vậy dạng tồn tại của carbene phụ thuộc
3 yếu tố:
- nó được hình thành bằng cách nào?
- Tốc độ pu nhanh hay chậm
- Nó có khả năng chuyển sang dạng khác của carbene(triplet hay singlet).



