Trích:
Nguyên văn bởi mystickharin

Cho mình hỏi khi 2 cấu tử hòa tan hoàn toàn vào nhau thì dung dịch thu được có nhiệt độ ngưng tụ so với nhiệt độ sôi như thế nào?Lớn hơn, nhỏ hơn hay bằng?
|
- Nhiệt độ sôi của hỗn hợp thấp hơn nhiệt độ sôi của các cấu tử
Hệ gồm 2 cấu tử và 2 pha nên theo quy tắc pha:
f = k – Φ + 2 = 2 – 2 + 2 = 2
Hệ có 2 bậc tự do, trong đó có các yếu tố: p, T, nồng độ (yA, yB với Σyi = 1; xA, xB với Σxj = 1). Ta xét cân bằng pha của hệ lỏng – hơi theo đồ thị pha:
* P = const : y* = f(x)
* P = const : t – x,y
* t = const : p – x,y
* Đối với hỗn hợp lỏng – hơi lý tưởng có T < Tth tuân theo định luật Raoult:
pi* = pi0.xi - pi* và pi0 đo ở cùng nhiệt độ
xết hệ 2 cấu tử A,B:
pA*=PA0.XA;pB*=PB0.(1-XA)
áp suất chung:P=pA*+pB*=PA0.XA+PB0.(1-XA)
=>y*A=pA*/P=(PA0.xA)/P=(PA0.xA)/[PA0.xA+PB0.(1-xA)]=
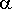
xA/[
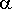
xA+(1-xA)
y*A=
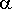
xA/[1+(
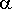
-1).xA hay
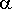
=[y*.(1-x)]/[x*.(1-y)]
với
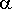
=PA0/PB0 là độ bay hơi tương đối của A đối với B
- Hỗn hợp có sai lệch dương so với định luật Raoult:
* Sai lệch dương: hỗn hợp có áp suất tổng lớn hơn áp suất tính theo định luật Raoult:
P = pA + pB > pA0.xA + pB0.xB
* Đặc điểm: có điểm đẳng phí ứng với nhiệt độ sôi cực tiểu
* Hệ điển hình:
Hệ ethanol - nước có điểm đẳng phí ở 1 at ứng với 89,4%mol ethanol, sôi ở 78,2 0C
- Hỗn hợp có sai lệch âm so với định luật Raoult:
* Sai lệch âm: hỗn hợp có áp suất tổng nhỏ hơn
áp suất tính theo định luật Raoult:
P = pA + pB < pA0.xA + pB0.xB
* Đặc điểm: có điểm đẳng phí ứng với nhiệt độ sôi cực đại
* Hệ điển hình:
Hệ HCl - nước có điểm đẳng phí ở 1 at ứng với 11,% mol HCl, sôi ở 110 0C
* Hỗn hợp 2 chất lỏng không tan vào nhau:
- Đặc điểm:
P = pA + pB = PA0 + PB0 > PA0, PB0
- Nhiệt độ sôi của hỗn hợp thấp hơn nhiệt độ sôi của các cấu tử



