Bổ sung thêm cho bác schrodigre:
S dc gọi là entropi là đại lượng đặc trưng cho độ mất trật tự của hệ trong phản ứng, S càng lớn thì độ mất trật tự càng cao phản ứng xảy ra càng dễ và ngược lại
Thêm 1 chút nữa, hiện tại người ta kô dùng cách sida nữa
.gif)
, vì cách nì can thiệp thô bạo vào CT đại số, trước phản ứng kô có Q mà sau phản ứng lại có Q mà lại còn cộng trừ nữa nên nó kô dc chấp nhận
Còn cái định luật Hess, có thể hiểu như thía nì:
VD: C(r) + 1/2O2 (k) --> CO(k)
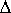
H1 = -110,5kJ
CO(k) + 1/2O2(k) --> CO2(k)
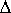
H2 = -283,0 kJ
C(r) + O2(k) --> CO2(k)
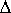
H3 = -393,5kJ
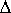
H3 =
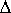
H1 +
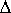
H2
Nhiệt tạo thành của phản ứng tổng cộng chỉ là nhiệt của phản ứng tạo thành CO2 từ C(r) và O2(k), kô phụ thuộc vào quá trình tạo CO



