Câu 1: Số mol của Ar: n = 0,02 mol.
Xét hai quá trình:
1. Quá trình giãn nở đẳng nhiệt ở 298K từ 500 ml tới 1000ml
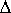
S(1) = 0,02.8,314.ln2= 0.11526 J/mol
2. Quá trình đẳng tích, khối khí có nhiệt tăng từ 298k tới 373K.
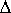
S(2) = 12,48.ln(373/298) = 0.056 J/mol
Do đó biến thiên entropy của cả quá trình là:
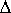
S = 0.11526 + 0.056 =0.1713 J/mol
Câu 2:
a, Áp dụng công thức biến thiên entropy cho quá trình giãn nở đẳng nhiệt của một khí:
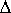
S = nR.ln(V2/V1).
Coi quá trình trộn lẫn hai khí là quá trình giãn nở đẳng nhiệt của từng khí và cộng các giá trị biến thiên entropy của hai khí ta được hệ thức như đáp án.
b, Ráp số vào có kết quá (lưu ý: NA, NB là nồng độ phần mol của A, B trong hỗn hợp sau cùng.
c, Tất nhiên là biến thiên entropy bẳng 0 rồi. Nồng độ phần mol của nó bằng 1 mà.
Câu 3: Áp dụng công thức ta có:
H = nRT.ln(P2/P1) = 2.8,314.298.ln0,1 = 11409.64 J



