Câu hỏi thảo luận rất hay, nhưng ko hiểu sao bạn Phương lại ko theo tới cùng để clearly vấn đề, hay là bạn đã clearly rùi thì cũng đáng mừng, nhưng cũng đáng trách là tại sao ko share những kíên thức đó lên đây để BM cùng anh em sáng tỏ luôn chứ !!! hehehe !
Vì câu hỏi này hình như cũng là bức xúc của nhiều sinh viên 04, rất mù mờ khi ko biết sử dụng bất kì thuyết gì để predict độ bền tương đối của phức, lí do khách quan lẫn chủ quan đều có !!!
@chú hai: Mày nói ko có thuyết nào giúp dự đoán độ bền là tao ko đồng ý, và người ta cũng viết báo đầy ra kia, chứ ko phải ko có bài báo nào về cái độ bền của phức đâu !!!
@All: bây giờ BM sẽ viết một bài đi vào bản chất của độ bền (gần tuyệt đối) và phương pháp dự đoán độ bền tương đối của các phức với các cấu trúc quen thuộc là tứ diện (tetrahedral) và bát diện (octahedral). Mong nhận được sự thảo luận của nhiều bạn trong khối 04 đang học !
Quả thật trong hai thuyết được học
VB với
Ligand Field, ko có thuyết nào đưa ra được cái nhìn bằng mô hình chính xác 100% cho tất cả các phức chất được, cho nên, để bắt đầu cái topic này (đuợc xem như bản chất), BM bắt đầu từ những
giản đồ MO của phức chất
!
Phương pháp MO có thể nói đã thành công trong việc đưa ra hình ảnh tổng quan, hoàn thịên nhất về phức chất, ngay trong giản đồ của nó, đã
bao gồm luôn hai thuyết nổi tiếng VB và LF. Một vài ví dụ nhé !!!
Xét sự tạo thành đơn giản nhất của một phức chất MXn , với X là bộ Ligand ko tạo được liên kết pi (NH3 và H2O), và M là một nguyên tử trung tâm bất kì như Ti3+ hay Cr3+ …
Trong MO, tất cả các AO của các nguyên tử đều phải tham gia tổ hợp, nhưng ở đây, ta chỉ thừa nhận những AO hoá trị tham gia chủ yếu vào sự tổ hợp, ảnh hưởng trực tiếp đến cấu hình phức chất.
a. Nguyên tử trung tâm có 9 AO tham gia tổ hợp (1AO s + 3AO p + 5AO d)
b. Mỗi Ligand đóng góp 4 AO (1AO s + 3AO p), có nghĩa là tổng số Ligand đóng góp 4n AO.
Hình minh hoạ đẹp đê !!!
MX6:

Trên hình đã phân chia rất rõ ràng thành hai cột, và mỗi AO của metal đều tương ứng với một bộ AO đối xứng của Ligand. Cột bên trái mô tả các cặp đối xứng của các AO s và p của Metal. Cột bên phải mô tả các cặp đối xứng của các AO d của metal.
Thực hiện sự tổ hợp, ta sẽ có giản đồ sau:

Nhìn vào giản đồ, ta thấy, những
MO bonding nằm trong phạm vi vạch màu vàng chính là hình ảnh của thuyết VB, và
các MO tổ hợp trong vùng được tô màu xanh da trời là hình ảnh của LF theory, có sự tách mức năng lượng
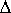
o. Hai MO của Ligand Field, một MO là sự tổ hợp
antibonding của eg, một là
MO nonbonding t2g .
Như vậy, ta đã phần nào thấy rõ được sự lợi hại của MO, nó là hình ảnh toàn diện nhất, hoàn chỉnh nhất của hệ thống, ko bỏ qua Ligand như Ligand Field, và cũng ko phớt lờ những MO antibonding như VB.
Tiếp theo, ta sẽ dùng
MO giải thích dãy phổ tác dụng trường trong Ligand Field, tại sao
các anion halogen lại có trường yếu hơn các phân tử trung hoà như H2O, NH3, mặc dù bản chất của thuyết LF chính là sự tương tác giữa Ligand với lớp vỏ electron d của center atom, làm phân tách năng lượng các AO thành các mức khác nhau. Và tại sao, những anion Ligand tổ hợp như CO, CN-, NO+, PF3 …
Ví dụ, xét phức của nguyên tử trung tâm Cr(3+), với lần lượt 3 bộ Ligand NH3, Cl- , CO. Các phức trên đều có cấu trúc bát diện MX6, như vậy, số AO tham gia tổ hợp:
+ Nguyên tử trung tâm có 9 AO tham gia tổ hợp (1AO s + 3AO p + 5AO d)
+ Mỗi Ligand đóng góp 4 AO (1AO s + 3AO p), có nghĩa là tổng số Ligand đóng góp 4n AO = 24 AO
Với lập luận tổ hợp đối xứng như ở trên, ta có thể đưa ra nhanh các giản đồ:



Nhìn vào ba giản đồ trên, ta phải đặc biệt chú ý đến năng lượng tách trường phối tử, nếu như ở giản đồ của bộ Ligand NH3 , ta thấy,
MO hạ năng của trường phối tử chính là MO nonbonding của metal, trong khi nếu xét bộ Ligand Cl-, anion Cl- có khả năng tạo phức pi phụ với nguyên tử trung tâm, bằng cách phối trí electron ở orbital p (hoặc d) vào orbital bộ 3 AO dxy, dyz, dxz của metal, và cũng tương tự trong trường hợp với bộ Ligand CO, nhưng ngược lại, nguyên tử trung tâm tạo liên kết pi phụ với Ligand bằng cách phối trí electron ở bộ 3 AO (dxy, dyz, dxz) vào orbital group antibonding của CO:

Điểm khác nhau duy nhất từ hai sự tổ hợp này chính là
năng luợng ban đầu của các AO và MO group tham gia tổ hợp. Trong trường hợp của Cl-, ta thấy AO p của Cl- có năng lượng thấp hơn AO d của metal, do vậy, sự tổ hợp làm giảm năng lượng tách trường. Trong khi trường hợp của CO, AO d của metal phải tổ hợp với pi* CO có năng lượng cao hơn, và sẽ tạo ra hai MO trường phối tử có năng lượng tách lớn hơn:

Vậy là ta đã giải thích xong dãy phổ được đề nghị bằng thực nghiệm ở LF theory, MO lợi hại thiệt, anh em hỉ !!!
Bây giờ ta đã có đủ cơ sở để trở về câu hỏi của bạn Phương, khi xét độ bền của phức, ta phải dựa vào yếu tố nào !?
Nhìn vào giản đồ MO, đương nhiên, độ bền của phức phụ thuộc vào sự tổ hợp hiệu quả của các AO và MO group ban đầu. Sự tổ hợp càng hiệu quả, sẽ tạo ra các MO bonding có năng lượng thấp hơn năng lượng trung bình của phức càng nhiều, và song song là sự tăng năng lượng của các MO antibonding càng cao, phức càng bền. Khi dùng giản đồ MO để định tính, tức là trước tiên, ta phải xét đến sự tổ hợp hiệu quả, gồm những luận điểm tạo liên kết bền trong VB, đó là tính đối xứng của các orbital tổ hợp, sự đồng năng của các orbital tổ hợp, mật độ xen phủ và vùng xen phủ (hix, cái này anh em phải hiểu là BM đã đơn giản hoá đi rất nhiều về MO). Sau đó, ta mới xét đến yếu tố tách trường phối tử, chẳng hạn như trong trường hợp của bộ Ligand CO và Cl- chẳng hạn, rõ ràng khi electron điền vào MO hạ năng của trường phối tử ở CO sẽ làm bền hệ thống hơn ở Cl-.

và điều này cũng xảy ra tương tự với phức tứ diện:

Như vậy, ta đã hoàn tất xong bản chất của sự làm bền phức chất. Bây giờ có hai bài tập nho nhỏ anh em thảo luận cho vui:
1.So sánh độ bền của các phức [Hg(Cl)4](2-), [Hg(Br)4](2-), [Hg(I)4](2-)
2.So sánh độ bền của các phức sau: [Co(H2O)6](2+), [Co(H2O)6](3+), [Co(NH3)6](2+), [Co(NH3)6](3+), [Co(F)6](3-), [Co(CN)6](3-).
Chỉ cần định tính với lập luận logic, rồi sau đó anh em nghía thêm bảng thực nghiệm, sẽ rõ hơn.
Chúc anh em ngon miệng với hai bài ăn tối !!!
@all: Còn rất nhiều vấn đề về phức chất nữa, anh em 04 cứ nêu ra để thảo luận nhé !!!



